با یکی دیگر از مقالات شرکت اعتماد تجارت کیهان وارد کننده ایمپلنت های دندانی درباره خواندنیهای کاشت ایمپلنت همراه باشید، در این مقاله به تاثیرگذار بر میکروبیوتای زیرلثه ای دور ایمپلنت ها خواهیم پرداخت.
ریززیواگان یا میکروبیوتا (به انگلیسی: Microbiota) باکتریهایی که به طور طبیعی در حفره دهانی زندگی می کنند (یعنی میکروبیوتای بومی) میتواند از میان اکوسیستمهای مختلف برای زیستگاه خوب انتخاب کنند. براساس معیارهای فیزیکی و مورفولوژیکی، حفره دهانی را میتوان به پنج اکوسیستم اصلی (که نیز نیچ نامیده می شود) تقسیم نمود، و هر یک شاخص های اکولوژیکی مجزایی دارند
- اپیتلیوم دهانی
- پشت زبان
- سطح دندان زیرلثهای
- جیب پریودونتال (دارای مایع گردنیاش، سمنتوم ریشه و اپی تلیوم جیب)
- لوزهها
اکثر گونههای پاتوژنیک (به استثنای اسپیروکت ها که خود را محدود به جیب میکنند) قادر به کلنیسازی در کلیه نیچها میباشند. برخی پریودونتوپاتوژن ها (P. intermedia, F. nucleatum) در سبب شناسی لوزهها دخیلاند درحالیکه سایرین حتی در سینوسهای فک بالایی کلنیسازی میکنند. حتی در دهان بیدندان اطفال یا افراد دارای دندان مصنوعی، نسبتهایی از پریودونتوپاتوژنها (به استثنای A. actinomycetemcomitans و P. gingivalis) میتواند بالا باشد. چون اکثر پاتوژنها در بیش از یک نیچ یافت میشوند، منطقی است فرض کنیم که انتقال میان این نیچ های درون دهانی (به نام جابه جایی) رخ می دهد.
 |
وجود چنین جابهجایی با مزایای بالینی و میکروبیولوژی عفونت یک مرحلهای کامل دهان یا یک برنامه ریزی ریشه یک مرحه کامل دهان هنگام مقایسه با یک درمان پریودونتال استاندار (ربع به ازای ربع) شرح داده شده است. نیز توضیح میدهد که چرا بازسازی هدایت شده بافتی زمانی که در یک حفره دهانی با یک بار میکروبی کاهش یافته اجرا میشود موفقیت آمیزتر است و چرا کاربرد آنتی بیوتیکهای موضعی به ویژه زمانی که کلیه جیبهای پاتوژنیک در درمان دخیل هستند، موفقیت آمیز است.
در همه این شرایط، حذف پاتوژنیکترین گونهها از حفره دهانی حلقی در عرض یک دوره کوتاه زمانی به طور معنی داری شانس جابجایی های باکتریایی درون دهانی را کاهش می داد. جیب های پریودونتال نقش قطعی را به عنوان مخازن میکروبی بازی میکنند. در واقع، بعد از یک دندان کشی کامل، اغلب پریودونتوپاتوژنها از حفره دهانی ناپدید میشوند.
 |
جیبهای پری ایمپلنت در بیماران نیمه بیدندان
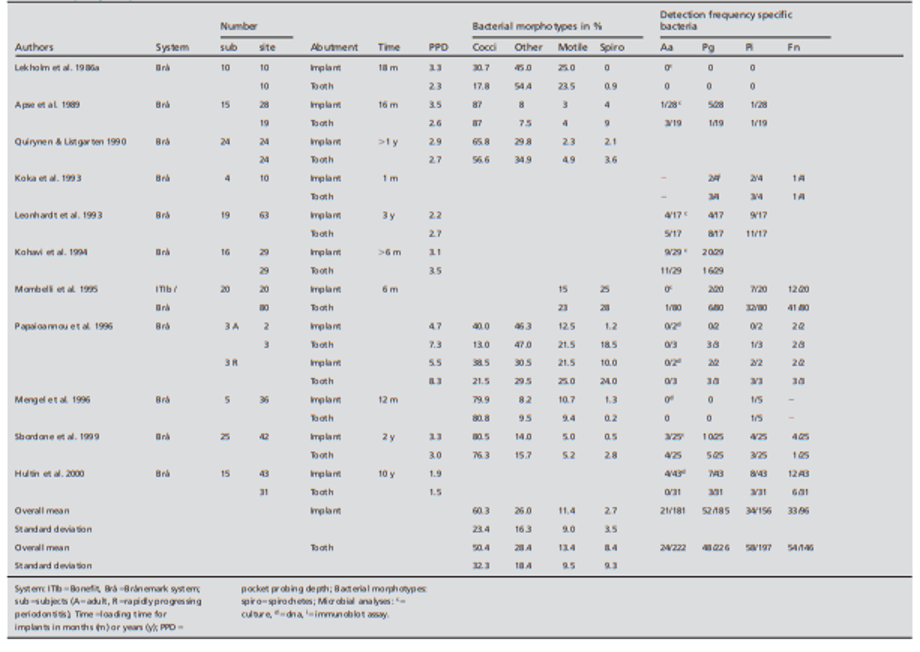
چنین جابه جایی داخل دهانی باکتریها البته توضیح میدهند که چرا گونههای پاتوژنیک منشا گرفته از جیبهای پریودونتال در جیبهای پری ایمپلنت در بیماران نیمه بیدندان کلنی سازی خواهند کرد. در واقع، مطالعات در اوایل دهه 90 توسط Apse و همکارانش در 1989 و Quirynen & Listgarten در 1990 نشان دادند که دندانهای باقیمانده در بهویژه بیماران بی دندان به شکل مخازنی برای کلنی سازی ایمپلنتهای نصب شده اخیر (جدول شماره ۱) عمل میکنند.
این شباهت در میکروفلور میان دندانها و ایمپلنتها در بیماران نیمه بیدندان از آن موقع توسط چندین مطالعه تایید شدهاند، بهویژه زمانی که عمق پروب گذاری حول هر دو نوع اتصال قابل مقایسه بوده است (جدول شماره ۱). نسبت اسپیروکتها و ارگانیسمهای متحرک دور هر دو نوع اتصال و تعداد واحدهای تشکیل دهنده کلنی مشابه میباشند. حتی در فراوانی شناسایی گونه های پاتوژنیک تنها تفاوتهای اندکی میان هر دو نوع اتصالها میتوانست شناسایی گردد (جدول شماره ۱). این شباهت خیلی زود پس از نصب ایمپلنت ظاهر میگردد. Leonhardt و همکاران (1993) پریودونتوپاتوژنهایی را در محیط پری ایمپلنت زیرلثهای بالواقع یک ماه بعد از ارتباط اتصال شناسایی کردند. کلیه مطالعات جدول شماره ۱ این مفهوم را تایید میکند که میکروفلورهای حاضر در حفره دهانی قبل از نصب ایمپلنت ترکیب میکروفلورهای تازه نصب شده دور ایمپلنتها را تعیین میکند. دومی نیز در مطالعه ای تایید گردید که در آن حضور 23 گونه زیرلثهای دور هر دو دندانها و ایمپلنتها از طریق کل پروبهای DNA ژنومیکی در یک بررسی صفحه شطرنجی بررسی گردید.
تاثیر پریودونتال دندانهای باقیمانده بر ترکیب فلور زیرلثهای دور ایمپلنت
وضعیت پریودونتال دندانهای باقیمانده بر ترکیب فلور زیرلثهای دور ایمپلنتها اثر می گذارد. زمانیکه ۳۱ بیمار نیمه بیدندان با شرایط مختلف پریودونتال برای دندان درآوری طبیعی بررسی گردید، میکروسکوپ فاز کانتراست فرضیه انتقال را تایید کرد. با رفتن از حالت سالم به پریودونتیت مزمن تا صعب العلاج، تعداد سلولهای کوکوئیدی به طور معنی داری در جیبهای دور هم دنداها و هم ایمپلنتها کاهش یافتند درصورتیکه تعداد اسپیروکت ها و جنبده ها به طور معنی داری برای هر دو نوع اتصال حتی بالای ۲۰ درصد سطح آستانه برای بیماری افزایش یافت.
یک تحلیل DNA فقدان مشکوک چترین پریودونتوپاتوژن ها را (P. gingivalis, Treponema denticola, C. rectus ) در گروه سالم نشان دادند، اما یک شناسایی مکرر آنها دور هر دو دندانها و ایمپلنتها در گروه مزمن و بویژه در گروه صعب العلاج دست کم در جیب های عمیق را نشان دادند. Sanz و همکاران (1990) بیماران نیمه بی دندان را که با ایمپلنتهای سرامیکی یاقوت کبود اندوستئال بازتوانی شده بودند بررسی کردند و تعداد و درصد معنی دار بالاتری از پریودونتوپاتوژنهای مشکوک را دور ایمپلنتها و دندانها با علائم التهاب ژینژیوال مشاهده نمودند. در این مکانهای بیمار، نسبت میلهایهای غیرهوازی گرم منفی به 40 درصد افزایش یافت.
زمانی که بیماران نیمه بیدندان به بیماران کاملا بدون دندان (بدون دندانهای باقیمانده در هر دو فک اما بازتوانی شده با ایمپلنت ها) مقایسه می شوند، اثر دندانهای باقیمانده حتی برجسته تر میشود. بیماران کاملا بدون دندان بازتوانی شده (جدول 3) با نسبت پایین تر معنی دار ارگانیسم های متحرک (3 درصد در مقابل 11.4%) و اسپیروکت ها (0.9% در مقابل 2.7%) و فراوانی های شناسایی خیلی پایین برای گونه های پاتوژنیک مشخصه سازی می گردند.
در این 6 مطالعه روی بیماران کاملا بیدندان که با ایمپلنتها بازتوانی گردیدند. P. gingivalis و A. actinomycetemcomitans هرگز نتوانستند شناسایی گردند (0/75). فراوانی شناسایی برای P. intermedia (7/75) نیز به نظر میرسد که کاهش یافته است اما برای F. nucleatum چنین نیست. Lee و همکارانش (1999b) میکروتوبیای زبان، دندان ها (اگر وجود داشته باشد) و ایمپلنتها، ایمپلنت گذاری قبل و بعد در بیماران نیمه بی دندان و کاملا بی دندان (با استفاده از پروب های DNA ژنومی کل) بررسی کردند. آنان یک تشابه بزرگی را در ترکیب پلاک بین نمونه ها از 3 نیچ فوق مشاهده نمودند و نتیجه گیری کردند که در کنار دندانها، زبان نیز باید به عنوان یک منبع باکتری اضافی در نظر گرفته شود. تشابه در ترکیب پلاک زیرلثه ای بین ایمپلنتها و دندانهای مجاور بزرگترین بوده است. مشاهدات دال براینکه ایمپلنتها در بیماران کاملا بیدندان یک فلور زیرلثهای مشابه با مال سطح مخاطی مجاور را پناه میدهند، نیز توسط مطالعه ای از Danser و همکارانش(1997) مورد تایید قرار گرفت. Smedberg و همکارانش (1993) 18 نفر را با دندان مصنوعی درآوردنی در فک بالایی بررسی کردند و نتوانستند تفاوتهای معنی داری را در الگوی ترکیب میکروبی جیب پری ایمپلنت و مال بیوفیلم روی طرف مخاطی منطبقه پروتز فک بالا شناسایی کنند.
کلیه دادهها تایید کننده این مفهوم است که باکتریهای کلنیساز در ایمپلنت ها در بیماران بی دندان اساسا از سطح غشای مخاطی دهانی منشا گرفتهاند یعنی میکروبیوتای حاضر در حفره دهانی قبل از ایمپلنت گذاری.
چندین مطالعه نشان میدهد که بالواقع یک ماه بعد از دندان کشی کامل، A. actinomycetemcomitans و P. gingialis نتوانستند دیگر شناسایی گردند. داده های جدول 3 نیز حاکی از آن است که حتی پس از جایگزینی دندانها با پروتزهای حمایت شده با ایمپلنت، A. actinomycetemcomitans و P. gingivalis زیر سطح شناسایی باقی می مانند و بطور دائمی از حفره دهانی ناپدید شده اند. طی برنامه درمان این امر بحثی برای کشیدن یک دندان دچار پریودونتیت پیشرفته پیش می آورد، چون جیب میتوانست به مشکل مخزن برای گونه های پاتوژنیک کلنی سازی کننده در ایمپلنت عمل کند.
عمق جیب پروب گذاری
طی نصب اتصال (ایمپلنت های دومرحله ای) یا طی واردسازی ایمپلنت (سیستم های تک مرحله ای)، پریودونتولوژیست در مورد عمق جیب پری ایمپلنت آتی با کوتاه کردن بیش از کم دریچه موکوپریوستئال و/یا با استفاده از یک مجموعه بهبودی بعد از جراحی برای حفظ اندکی فشار طی بهبودی تصمیم گیری میکند. تا کنون، اهمیت عمق جیب پروب گذاری دور ایمپلنت دهانی توجه زیادی را دریافت نکرده است. اخیرا، Papaioannon و همکارانش (1995) رابطه میان فلور میکروبی زیرلثه ای اطراف ایمپلنت های موفق و پارامترهای پریودونتال آنها را بررسی کردند. نمونه های پلاک از 561 ایمپلنت بوسیله میکروسکوپ فاز کنتراست افتراقی یا DPCM تحلیل گردیده و با عمق پروب گذاری محل نمونه، تمایل به خونریزی هنگام پروب گذاری و شاخص های پلاک و ژینژیویت مقایسه گردیدند. از این پارامترهای بالینی تنها عمق پروب گذاری به طور نزدیکی با پاتوژنیسیته مشخص گردید که فلور میکروبی مرتبط می باشد؛ هر چه جیب عمیق تر باشد، نسبت اسپیروکت ها و ارگانیسم های جنبنده بالاتر است. در یک مطالعه دیگری، مشاهده گردید که فلور میکروبی زیرلثه ای دور ایمپلنت ها در بیماران نیمه بی دندان دارای پریودونتیت مزمن مادامی که جیب ها عمق زیر 4 میلی متر داشته باشند، غیرپاتوژنیک باقی می مانند. این مشاهدات هماهنگ با مطالعاتی است که به یک رابطه مثبت بین عمق پروب گذاری اطراف دنداانها و تناسب اسپیروکت ها اشاره کرده اند.
اثر عمق پروب گذاری روی میکروبیوتای زیرلثه ای نیز برای ایمپلنت های ITI یک مرحله ای توسط Mombelli & Mericske-stern گزارش گردید. آنها مشاهده کردند که نسبت نسبی Capnocytophaga و A. odontolyticus دور ایمپلنت ها که از چیزهای بیش از حد در بیماران بی دندان حمایت می کند به طور مثبتی با عمق پروب گذاری همبستگی داشت. سایرین گزارش یک همبستگی مثبت را بین عمق پروب گذاری و رخداد/نسبت اسپیروکت ها، باکتری های هیدرولیز کننده BANA، یا گونه های غیرهوازی (برای سیستم های ایمپلنت مختلف) داده اند. George و همکاران (1994) یک همبستگی مثبت را میان عمق پروب گذاری و/یا زمان تماس داخل دهانی و حضور P. gingivalis ،P. intermedia و A. actinomycetemcomitans گزارش دادند. این مشاهدات باید پریودونتولوژیست را تشویق کنند تا از حضور جیب های پری ایمپلنت عمیق طی جراحی مرحله دوم دست کم زمانی که زیبایی شناسی و آواشناسی امکان آنرا می دهد، جلوگیری کند. اما کوتاه سازی بافتهای نرم نباید فراتر از 3 میلیمتر باشد چون در حیوانات دست کم وجود یک عمق بیولوژیکی حداقل به خوبی مستندسازی شده است.